L’INFLUENCE DU DHA SUR NOTRE INTESTIN
Les nombreux avantages des oméga-3 sont connus depuis longtemps, mais dans de nombreux cas, le mécanisme par lequel ils ont des effets positifs est moins clair. De récentes recherches commencent à démontrer que certains de ces effets pourraient être dus à l’influence des oméga-3 sur les micro-organismes vivant dans nos intestins. Le microbiome intestinal humain est l’ensemble des micro-organismes (microbiote) présents dans le tube digestif humain. Il s’agit d’un écosystème interconnecté de bactéries, de levures et d’autres organismes tels que les protistes, les archées et les virus.
Le microbiome intestinal est le plus grand réservoir de micro-organismes du corps humain et contribue en grande partie à l’activité enzymatique essentielle à la digestion et à la physiologie humaine.
Le microbiote et son hôte humain sont un exemple de symbiose mutualisée, dont les deux parties tirent pleinement avantage. Plusieurs facteurs influencent la composition du microbiote, tant au niveau des types d’organismes présents que de leur abondance, ce qui rend les profils de microbiote intestinal très spécifiques à chaque hôte.
Le régime alimentaire est l’un des facteurs les plus influents sur la composition et la stabilité du microbiote intestinal, mais d’autres facteurs tels que l’âge, le sexe, la masse corporelle, les choix de mode de vie et la fonction immunitaire peuvent avoir un impact important, tout comme les facteurs environnementaux liés, par exemple, à la situation géographique. L’utilisation d’antibiotiques, de drogues, d’alcool et de probiotiques peut également avoir un impact important sur le microbiote.
Lorsque notre flore intestinale est déséquilibrée, nous parlons de dysbiose. Il y a alors un changement dans la composition ou la stabilité des populations bactériennes de l’intestin qui altère la relation symbiotique. Cette situation peut être causée par de nombreux facteurs tels que l’utilisation d’antibiotiques, une maladie ou une mauvaise alimentation, et elle peut avoir des conséquences à long terme sur la santé.
Un microbiote dysbiotique peut être associé à des troubles métaboliques tels que le diabète de type 2, l’obésité ou les maladies cardiovasculaires, et certains composants d’un microbiote déséquilibré ont été associés à des maladies inflammatoires chroniques de l’intestin telles que la maladie de Crohn ou la colite ulcéreuse, ainsi qu’au développement d’allergies et du cancer colorectal.
Restauration du microbiote et reduction de l’inflammation intestinale grâce à l’huille issus de microalgues
On pense que certains troubles métaboliques de l’hôte sont associés à une composition du microbiote intestinal ayant une influence anormale sur l’inflammation. Les différentes bactéries présentes dans l’intestin peuvent modifier la fonctionnalité immunitaire et jouer des rôles pro- et anti-inflammatoires.
Ainsi, la composition du microbiote influence le niveau de résistance de l’hôte aux infections et à sa sensibilité aux maladies inflammatoires. Les acides gras polyinstaurés issus des oméga-3 exercent des effets significatifs sur l’environnement intestinal en agissant sur la composition du microbiote intestinal, favorisant une augmentation des groupes qui produisent des composés anti-inflammatoires, comme les acides gras à chaîne courte (1,2).
Les antibiotiques peuvent être particulièrement perturbateurs pour le microbiote, surtout au début de la vie, et les oméga-3 peuvent atténuer les problèmes qu’ils peuvent causer, et réduire les risques dû à un déséquilibre, comme l’obésité (2). Dans une étude récente, Yang et al. ont étudié l’effet des huiles issus de microalgues, riches en DHA, sur la dysbiose causée par un traitement antibiotique.
Un traitement à base d’huile algal (500 mg kg-1 jour-1) a rétabli l’équilibre du microbiote intestinal en augmentant le nombre de bactéries productrices d’acides gras à chaîne courte, telles que Ruminococcus et Blautia, et a réduit de manière significative les niveaux de cytokines pro-inflammatoires, notamment l’interleukine 6, l’interleukine 1β et le facteur de nécrose tumorale α, dans le côlon. Ils concluent que la supplémentation en huile algale pourrait atténuer l’inflammation et favoriser la cicatrisation des muqueuses, ce qui suggère que l’huile de DHA issu de microalgues pourrait être utilisée pour se protéger contre l’altération du microbiote intestinal et la dysbiose métabolique induites par les antibiotiques (3).
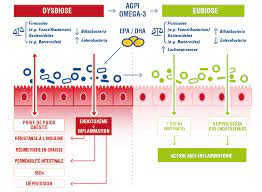
Figure 1 : Modifications du microbiote intestinal suite à la prise d’huiles oméga-3 permettant de réduire la dysbiose (3)
Le DHA influence l’axe intestin – cerveau
Le rôle structurel et fonctionnel important du DHA dans le maintien des fonctions cérébrales et nerveuses est bien connu; mais le microbiote intestinal peut également, de manière surprenante, avoir un effet sur le fonctionnement du cerveau via l’axe intestine – cerveau. Il y a un intérêt récent sur la possible interaction entre problèmes cérébraux et microflore intestinale; il a été démontré que les troubles émotionnels tels que la dépression, l’anxiété et le stress présentent une corrélation avec les altérations du microbiote intestinal (4). La colonisation bactérienne de différentes espèces peut potentiellement altérer les fonctions cérébrales et, à son tour, le système nerveux central, ce qui pourrait indirectement influencer la composition microbienne intestinale (5).
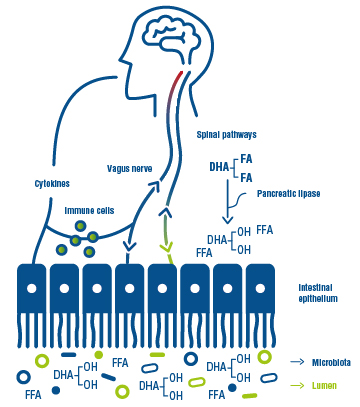
Figure 2 : Interactions entre l’intestin et le cerveau, le DHA jouant un rôle dans la composition du microbiote et des nerfs.
Les complements alimentaires à base de DHA peuvent avoir des effets bénéfiques sur les troubles comportementaux et neurophysiologiques non seulement par une action directe sur le cerveau, mais aussi en modifiant la composition microbienne de l’intestin, et donc par une action indirecte via l’axe sang-intestin. Il a été démontré que des niveaux circulants plus élevés de DHA sont en corrélation avec une meilleure diversité du microbiote (6). Il est intéressant de noter que les différences de prévalence de certains troubles mentaux entre les sexes peuvent également être liées à des différences dans le microbiote.
Des études menées sur des souris, par exemple, montrent que le DHA peut entraîner une réduction des symptômes d’anxiété et de dépression chez les mâles isolés socialement, mais pas chez les femelles; et ce phénomène est lié au microbiome (7).
Maladies inflammatoires chroniques de l’intestin et cancer colorectal
Les maladies inflammatoires chroniques de l’intestin, notamment la colite ulcéreuse et la maladie de Crohn, sont associées à une dysbiose du microbiome intestinal. Certaines données suggèrent aujourd’hui qu’elles peuvent également être liées à des déséquilibres du métabolisme des oméga-3 et des oméga-6, en particulier leur transformation en cytokines anti-inflammatoires ou inflammatoires (8). Bien que certains patients notent une diminution des symptômes suite à la prise d’oméga-3, les preuves de leur efficacité dans la gestion de ces maladies ne sont pas encore claires (9).
Néanmoins, il est clair que l’inflammation observée dans la colite ulcéreuse et la maladie de Crohn augmente le risque de cancer colorectal (CCR) au-delà de la moyenne générale. Le contexte pro-inflammatoire de ces maladies favorise pratiquement toutes les étapes de la carcinogenèse du côlon et les patients atteints de CCR présentent un niveau accru de médiateurs pro-inflammatoires circulants (IL-6, IL-1β, IL-8 et TNFα).
Des études épidémiologiques et cliniques montrent les effets anti-inflammatoires suite à la consommation d’acides gras polyinsaturés oméga-3 sur le risque de CCR, et l’on considère également qu’ils ont un rôle dans le traitement (10). Le rôle du DHA pourrait être lié à sa capacité à réguler la production de médiateurs pro-inflammatoires dans les cellules cancéreuses et/ou les cellules hôtes, modifiant ainsi le statut inflammatoire systémique ou celui du microenvironnement tumoral. Fluckiger et al. (12) ont démontré que le traitement au DHA induisait une inhibition de la croissance tumorale et une activation de l’apoptose dans les cellules cancéreuses du côlon par la voie du TNFα.
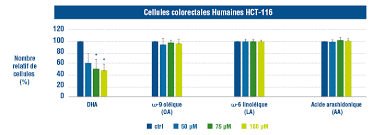
L’effet du DHA a été évalué sur la croissance des cellules cancéreuses du côlon humain (cellules HCT-116 et HCT-8) en utilisant le test Cyquant et comparé aux acides ω-9 oléique (OA), ω-6 linoléique (LA) et arachidonique (AA). Le traitement au DHA (50, 75 et 100 μM) pendant 48 h a réduit le nombre de cellules cancéreuses de manière dose-dépendante, tandis que le traitement à l’OA, à l’acide AA et au LA ne l’a pas fait par rapport au traitement témoin (CTRL) (Figures 2a et b) (11).
La population microbienne de nos intestins a un effet important sur de nombreux aspects de notre santé et de notre bien-être. Les antibiotiques, une mauvaise alimentation et d’autres éléments de notre mode de vie, comme le tabagisme et la consommation d’alcool, peuvent perturber l’équilibre délicat des espèces qui peuplent nos intestins.
Les oméga 3 ont un rôle avéré dans le rétablissement et le maintien d’un équilibre intestinal sain, et dans la réduction de l’inflammation des intestins. Le DHA favorise le développement des bactéries productrices d’acides gras à chaîne courte tout en réduisant les molécules pro-inflammatoires. Ces métabolites microbiens agissent comme un messager dans l’axe cerveau-intestin et sont corrélés à une réduction de l’anxiété et de la dépression.
En plus d’agir sur le microbiote, le DHA a un rôle potentiellement curatif en cas de cancer du côlon, dont le risque est accru par une inflammation chronique, en réduisant significativement le nombre de cellules cancéreuses.
Bibliographie :
- Costantini, L., Molinari, R., Farinon, B. & Merendino, N. Impact of Omega-3 Fatty Acids on the Gut Microbiota. Int. J. Mol. Sci. 18, E2645 (2017).
- Yawei Fu , Yadong Wang , Hu Gao, DongHua Li, RuiRui Jiang, Lingrui Ge, Chao Tong, and Kang Xu. Associations among Dietary Omega-3 Polyunsaturated Fatty Acids, the Gut Microbiota, and Intestinal Immunity. (2021)
- Kaliannan, K., Wang, B., Li, X.-Y., Bhan, A. K. & Kang, J. X. Omega-3 fatty acids prevent early-life antibiotic exposure-induced gut microbiota dysbiosis and later-life obesity. Int. J. Obes. 2005 40, 1039–1042 (2016).
- Yang, C. et al. Algal Oil Rich in Docosahexaenoic Acid Alleviates Intestinal Inflammation Induced by Antibiotics Associated with the Modulation of the Gut Microbiome and Metabolome. J. Agric. Food Chem. (2021) doi:10.1021/acs.jafc.0c07323.
- Taylor, A. M. & Holscher, H. D. A review of dietary and microbial connections to depression, anxiety, and stress. Nutr. Neurosci. 23, 237–250 (2020).
- Jin, J., Jin, Q., Wang, X. & Akoh, C. C. High Sn-2 Docosahexaenoic Acid Lipids for Brain Benefits, and Their Enzymatic Syntheses: A Review. Engineering 6, 424–431 (2020).
- Menni, C. et al. Omega-3 fatty acids correlate with gut microbiome diversity and production of N-carbamylglutamate in middle aged and elderly women. Sci. Rep. 7, 11079 (2017).
- Davis, D. J. et al. Sex-specific effects of docosahexaenoic acid (DHA) on the microbiome and behavior of socially-isolated mice. Brain. Behav. Immun. 59, 38–48 (2017).
- Scoville, E. A. et al. Serum Polyunsaturated Fatty Acids Correlate with Serum Cytokines and Clinical Disease Activity in Crohn’s Disease. Sci. Rep. 9, 2882 (2019).
- Turner, D., Shah, P. S., Steinhart, A. H., Zlotkin, S. & Griffiths, A. M. Maintenance of remission in inflammatory bowel disease using omega-3 fatty acids (fish oil): a systematic review and meta-analyses. Inflamm. Bowel Dis. 17, 336–345 (2011).
- Volpato, M. & Hull, M. A. Omega-3 polyunsaturated fatty acids as adjuvant therapy of colorectal cancer. Cancer Metastasis Rev. 37, 545–555 (2018).
- Fluckiger, A. et al. Inhibition of colon cancer growth by docosahexaenoic acid involves autocrine production of TNFα. Oncogene 35, 4611–4622 (2016).